協会の開発支援
協会の開発支援
協会の考える機能性表示食品の開発工程

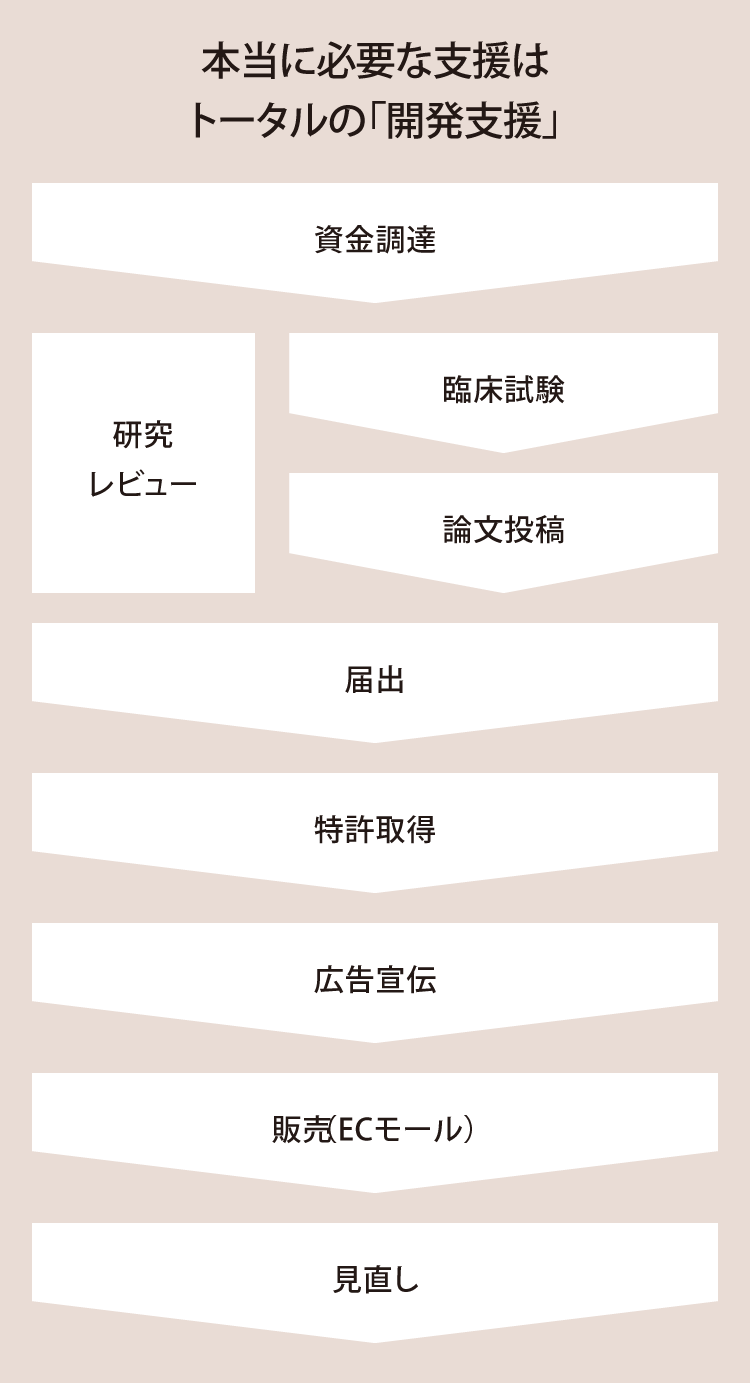
機能性表示食品の開発を検討する際、一般的には「商品開発」および「届出」の工程をに意識が集中してしまいますが、新商品を上市する上で開発段階から検討しておかなければならないそれ以外にもあると考えています。特に、新規顧客層の開拓を求めて、新たに健康食新市場に参入しようと考える企業様においては、「特許取得」や表示規制を遵守した「広告・宣伝」、ドラッグストア等への「販売」経路拡大など、解決しなければならない難題が山積みです。また需要が見込まれる食品素材はあるのだが、開発に取り掛かるまでの資金調達に苦労しているといった食品メーカー様、原材料メーカー様もいらっしゃることでしょう。
当協会は上市を見据えて機能性表示食品の開発を行いたいと考えるクライアント様の期待に応える開発支援メニューをご提案致します。
日本食品エビデンス協会の臨床試験開発体制
当協会は、医療機関との豊富なネットワークを駆使し、機能性表示食品の届出に必要なヒト試験を実施するためのご相談を承っております。
臨床試験の実施は、医薬品では当たり前となっている信頼性構築の手法に則り、届出事業者様をサポートするCROと医療機関様をサポートするSMOに組織を分け、公平性を保って実施しています。
開発業務受託機関(CRO)
<業務内容>
■ 臨床試験実施計画書等の臨床試験資材の作成
■ 割付及び統計解析
■ 試験報告書の作成
■ 論文投稿サポート
研究施設支援機関(SMO)
<業務内容>
■ 試験実施体制の構築
■ 被験者募集・スクリーニング
■ 同意説明・同意
■ 試験中の被験者管理
臨床試験の妥当性や健康被害の補償、個人情報保護に関する試験計画は、倫理審査委員会にて厳密に審査を行います。審査委員長は、大阪大学名誉教授 荻野敏先生が任命されています。
倫理審査委員会の設置

<業務内容>
■ 審査委員のアサイン
■ 臨床試験の審議
■ 審査委員会開催の事務作業
■ 審査結果報告書の作成
臨床試験を実施する研究機関は、対象となる機能性関与成分の特性ごとに選定されますが、MRIやCTなどのエビデンスの高い検査も実施可能である医療機関に依頼を行うよう心がけています。
臨床試験実施研究機関

<業務内容>
■ 臨床試験の実施
■ 各種検査の実施
■ 緊急搬送先との連携
■ 責任医師による投稿論文のチェック

